Đề kiểm tra học kỳ I Hóa học Lớp 12 - Năm học 2019-2020 - Có đáp án
Bạn đang xem tài liệu "Đề kiểm tra học kỳ I Hóa học Lớp 12 - Năm học 2019-2020 - Có đáp án", để tải tài liệu gốc về máy hãy click vào nút Download ở trên.
Tóm tắt nội dung tài liệu: Đề kiểm tra học kỳ I Hóa học Lớp 12 - Năm học 2019-2020 - Có đáp án
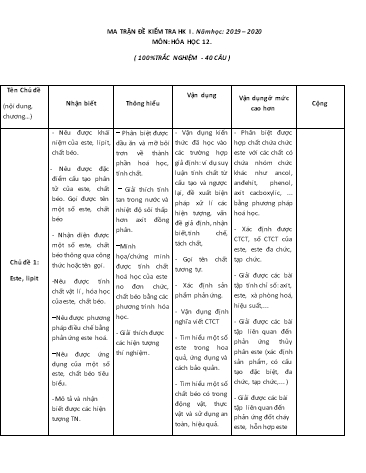
MA TRẬN ĐỀ KIỂM TRA HK I . Năm học: 2019 – 2020 MÔN: HÓA HỌC 12. ( 100% TRẮC NGHIỆM - 40 CÂU ) Tên Chủ đề Vận dụng Vận dụng ở mức Nhận biết Thông hiểu Cộng (nội dung, cao hơn chương) - Nêu được khái Phân biệt được - Vận dụng kiến - Phân biệt được niệm của este, lipit, dầu ăn và mỡ bôi thức đã học vào hợp chất chứa chức chất béo. trơn về thành các trường hợp este với các chất có phần hoá học, giả định: ví dụ suy chứa nhóm chức - Nêu được đặc tính chất. luận tính chất từ khác như ancol, điểm cấu tạo phân cấu tạo và ngược anđehit, phenol, tử của este, chất Giải thích tính lại, đề xuất biện axit cacboxylic, ... béo. Gọi được tên tan trong nước và pháp xử lí các bằng phương pháp một số este, chất nhiệt độ sôi thấp hiện tượng, vấn hoá học. béo hơn axit đồng đề giả định, nhận phân. - Xác định được - Nhận diện được biết,tinh chế, CTCT, số CTCT của một số este, chất tách chất, Minh este, este đa chức, béo thông qua công họa/chứng minh - Gọi tên chất tạp chức. Chủ đề 1: thức hoặc tên gọi. được tính chất tương tự. hoá học của este - Giải được các bài Este, lipit -Nêu được tính no đơn chức, - Xác định sản tập tính chỉ số: axit, chất vật lí , hóa học chất béo bằng các phẩm phản ứng. este, xà phòng hoá, của este, chất béo. phương trình hóa hiệu suất,... - Vận dụng định Nêu được phương học. nghĩa viết CTCT - Giải được các bài pháp điều chế bằng - Giải thích được tập liên quan đến phản ứng este hoá. - Tìm hiểu một số các hiện tượng phản ứng thủy este trong hoa thí nghiệm. phân este (xác định Nêu được ứng quả, ứng dụng và dụng của một số sản phẩm, có cấu cách bảo quản. este, chất béo tiêu tạo đặc biệt, đa biểu. - Tìm hiểu một số chức, tạp chức,... ) chất béo có trong - Mô tả và nhận - Giải được các bài động vật, thực biết được các hiện tập liên quan đến vật và sử dụng an tượng TN. phản ứng đốt cháy toàn, hiệu quả. este, hỗn hợp este Chủ đề 3: Xác định được Hiểu được các Viết được các Dựa vào đặc điểm CTCT và tên gọi của tính chất hóa học, phương trình, của phương trình Amin, các loại hợp chất, viết được phương tính toán trên tổng quát, tìm ra aminoaxit, phân loại các loại trình hóa học các phương trình quy luật và từ đó peptit, hợp chất phản ứng xảy ra, phản ứng. tính toán các chất protein xác định được các khác. chất tạo thành. Số câu 3 3 1 7 Khái niệm về Phân loại polime, Xác định được Chủ đề 4: polime, tên gọi phân biệt rõ các sản phẩm từ các Polime loại polime monome tương ứng Số câu 2 1 1 4 Phân biệt các loại Một số loại hợp Bài tập tổng hợp Bài tập sử dụng Chủ đề 5: hợp chất dựa vào chất có 1 số tên về một số loại kiến thức tổng hợp Tổng hợp hóa khái niệm hoặc tên phản ứng hóa học hợp chất nêu trên hóa hữu cơ để giải. hữu cơ gọi hay đặc điểm chung nhưng cấu tạo khác sản phẩm Số câu 3 2 1 2 8 Vị trí KL trong BTH, Hiểu được Dựa vào tính chất Dựa vào dãy điện Chủ đề 6: tính chất hóa học nguyên nhân gây hóa học của KL hóa, dựa vào tính Đại cương về của KL, vị trí các cặp nên tính chất vật làm các bài tập chất hóa học và các kim loại oxi hóa khử, các lý, nguyên nhân liên quan đến các kiến thức liên quan loại ăn mòn kim của sự ăn mòn phương trình để giải quyết các loại kim loại phản ứng xảy ra bài tập khó. Số câu 3 2 2 1 8 Tổng số câu 16 câu 12 câu 8 câu 4 câu Số câu: 40 Tổng số điểm 4đ 3đ 2đ 1đ Số điểm: 10 Tỉ lệ % 40% 30% 20% 10% Tỉ lệ 100% A. Glyxin.B. Tristearin. C. Metyl axetat.D. Glucozơ. Câu 13: Dung dịch nào sau đây không làm đổi màu quỳ tím? A. NaOH. B. H2NCH2COOH. C. HCl. D. CH3NH2. Câu 14: Tính chất hóa học đặc trưng của kim loại là A. tính bazơ. B. tính oxi hóa. C. tính axit. D. tính khử. Câu 15: Kim loại nào sau đây vừa phản ứng được với dung dịch HCl, vừa phản ứng được với dung dịch NaOH ? A. Fe.B. Ag.C. Cu. D. Al. Câu 16: Kim loại nào sau đây có nhiệt độ nóng chảy thấp nhất ? A. Na. B. Li.C. Hg. D. K. Câu 17: Khi thuỷ phân este E trong môi trường kiềm (dd NaOH) người ta thu được natri axetat và etanol. Vậy E có công thức là A. CH3COOC2H5 B. HCOOCH3. C. C2H5COOCH3 D. CH3COOCH3. Câu 18: Một este có công thức phân tử là C4H6O2, khi thuỷ phân trong môi trường axit thu được axetanđehit. Công thức cấu tạo thu gọn của este đó là A. CH2=CH-COO-CH3. B. HCOO-C(CH3)=CH2. C. HCOO-CH=CH-CH3. D. CH3COO-CH=CH2 Câu 19:Thủy phân hoàn toàn tinh bột trong môi trường axit, thu được chất nào sau đây? A. Glucozơ. B. Saccarozơ. C. Ancol etylic. D. Fructozơ. Câu 20. Tinh thể chất rắn X không màu, vị ngọt, dễ tan trong nước. X có nhiều trong cây mía, củ cải đường và hoa thốt nốt. Trong công nghiệp, X được chuyển hóa thành chất Y dùng để tráng gương, tráng ruột phích. Tên gọi của X và Y lần lượt là A. glucozơ và saccarozơ. B. saccarozơ và sobitol. C. glucozơ và fructozơ. D. saccarozơ và glucozơ. Câu 21: Cho các dung dịch: C6H5NH2 (anilin), CH3NH2, H2N-[CH2]4-CH(NH2)-COOH và H2NCH2COOH. Số dung dịch làm đổi màu phenolphtalein là A. 4. B. 3. C. 2. D. 1. Câu 22. Để phân biệt 3 dung dịch H2NCH2COOH, CH3COOH, C2H5NH2 ta cần dùng thuốc thử nào sau đây ? A. Dung dịch HCl. B. Dung dịch NaOH C. Natri. D. Quỳ tím. Câu 23: Thuốc thử được dùng để phân biệt Gly-Ala-Gly với Gly-Ala là A. dung dịch NaOH. B. dung dịch NaCl. C. Cu(OH)2 trong môi trường kiềm. D. dung dịch HCl. (b) Chất béo nhẹ hơn nước và không tan trong nước. (c) Glucozơ thuộc loại monosaccarit. (d) Các este bị thủy phân trong môi trường kiềm đều tạo muối và ancol. (e) Tất cả các peptit đều có phản ứng với Cu(OH)2 tạo hợp chất màu tím (g) Dung dịch sacarozơ không tham gia phản ứng tráng bạc Số phát biểu đúng là A. 5. B. 3. C. 4. D. 2. Câu 35: Hòa tan hoàn toàn Fe3O4 trong dung dịch H2SO4 loãng (dư), thu được dung dịch X. Trong các chất: NaOH, Cu, Fe(NO3)2, KMnO4, BaCl2, Cl2 và Al, số chất có khả năng phản ứng được với dung dịch X là A. 7. B.4. C. 6 D. 5 Câu 36: Cho 0,5 gam một kim loại hóa trị II phản ứng hết với dung dịch HCl dư, thu được 0,28 lít H2 (đktc). Kim loại đó là A. Ba.B. Mg. C. Ca.D. Sr. Câu 37: Cho 7,34 gam hỗn hợp E gồm hai este mạch hở X và Y (đều tạo bởi axit cacboxylic và ancol ; MX<MY<150) tác dụng vừa đủ với dung dịch NaOH, thu được một ancol Z và 6,74 gam hỗn hợp muối T. Cho toàn bộ Z tác dụng với Na dư, thu được 1,12 lít khí H 2. Đốt cháy hoàn toàn T, thu được H 2O, Na2CO3 và 0,05 mol CO2. Phần trăm khối lượng của X trong E là A. 81,74%. B. 40,33%. C. 30,25%. D. 35,97%. Câu 38: Hỗn hợp X gồm alanin, axit glutamic và axit acrylic. Hỗn hợp Y gồm propen và trimetylamin. Đốt cháy hoàn toàn a mol X và b mol Y thì tổng số mol oxi cần dùng vừa đủ là 1,14 mol, thu được H 2O; 0,1 mol N2 và 0,91 mol CO2. Mặt khác, khi cho a mol X tác dụng với dung dịch KOH dư thì lượng KOH phản ứng là m gam. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là A. 16,8. B. 14,0.C. 11,2. D. 10,0. Câu 39. Hỗn hợp E gồm 3 chất: X (là este của amino axit); Y và Z là hai peptit mạch hở, hơn kém nhau một nguyên tử nitơ (đều chứa ít nhất hai loại gốc amino axit, M Y < MZ). Cho 36 gam E tác dụng vừa đủ với 0,44 mol NaOH, thu được 7,36 gam ancol no, đơn chức, mạch hở và 45,34 gam ba muối của glyxin, alanin, valin (trong đó có 0,1 mol muối của alanin). Mặt khác, đốt cháy hoàn toàn 36 gam E trong O 2 dư, thu được CO2, N2 và 1,38 mol H2O. Phần trăm khối lượng của Y trong E là A. 18,39%. B. 20,72%. C. 27,58%. D. 43,33%. Câu 40: Điện phân dung dịch X gồm Cu(NO 3)2 và NaCl với điện cực trơ, màng ngăn xốp, cường độ dòng điện không đổi I = 2,5A. Sau t giây, thu được 7,68 gam kim loại ở catot, dung dịch Y (vẫn còn màu xanh) và hỗn hợp khí ở anot có tỉ khối so với H 2 bằng 25,75. Mặt khác, nếu điện phân X trong thời gian 12352 giây thì tổng số mol khí thu được ở hai điện cực là 0,11 mol. Giả thiết hiệu suất điện phân là 100%, các khí sinh ra không tan trong nước và nước không bay hơi trong quá trình điện phân. Số mol ion Cu2+ trong Y là A. 0,01. B. 0,02.C. 0,03. D. 0,04.
File đính kèm:
 de_kiem_tra_hoc_ky_i_hoa_hoc_lop_12_nam_hoc_2019_2020_co_dap.doc
de_kiem_tra_hoc_ky_i_hoa_hoc_lop_12_nam_hoc_2019_2020_co_dap.doc